مقدمه
آلکالوییدهای تروپان1 (TAs) ترکیبهای
شیمیایی هستند که بهطور
طبیعی و در اثر سوختوساز
ثانویه گیاهان تیرههای
شببویان، بادنجانیان
(از جمله مهرگیاه، بنگدانه،
شابیزک، داتوره) و اریتروکسیلاسه2 تولید میشوند.
این آلکالوییدها در همه قسمتهای
گیاه یافت میشوند و سمی بودن
گیاهان یاد شده به حضور آلکالوییدها در گیاه باز میگردد.
بهطور معمول غلظت آنها در ریشهها
و میوهها به بالاترین حد میرسد و با تغییرگونه،
فصل، موقعیت جغرافیایی و اندام گیاه تغییر میکند.
عصارههای
گیاهی دربردارنده TAs،
قرنها کاربرد دارویی
داشتهاند و هنوز هم به
عنوان داروهایی مهم در داروخانهها
عرضه میشوند. مردم بومی هند
برای درمان آسم، ریشه و برگهای
گیاه داتوره را میسوزاندند.
تنفس دود این گیاه اثر شگرفی در روند بهبود این بیماری داشت. درواقع معرفی
آلکالوییدهای تروپان به طب غربی از سوی استعمارگران بریتانیایی در دهه نخست1800 از
همین نقطه جهان شروع شد.
آلکالوییدهای تروپان در برابر گرما
کمابیش پایدارند. هنگامی
که از گندمهای آلوده به دانههای داتوره در پخت نان استفاده میکنیم، غلظت آلکالویید تروپان تا 28 درصد
کاهش مییابد. همچنین جوشاندن
آرد در تهیه انواع غذاها باعث کاهش غلظت
60 درصدی آتروپین و 40 درصدی اسکوپولامین3 میشود.
داتوره در مناطق معتدل و گرمسیری به فراوانی یافت میشود
و از آنجا که دانههای
آن همراه با فراورده های کشاورزی مهم از جمله بذر کتان، سویا، ارزن، آفتابگردان و
گندم سیاه برداشت میشود
برای این فراورده ها، ناخالصی خطرناکی بهشمار
میآید.
اگرچه بیش از دویست ترکیب در خانواده
آلکالوییدهای تروپان شناسایی شدهاند
اما اطلاعات همه آنها
در دسترس نیست و بیشترین بررسیها
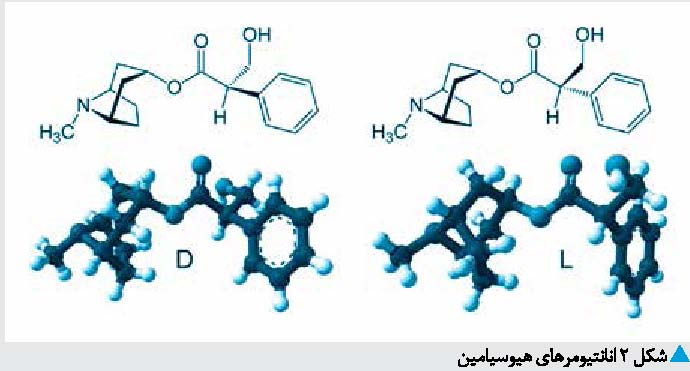
روی L-هیوسیامین4 و L-اسکوپولامین متمرکز شده است. مخلوط راسمیک از L- و D- انانتیومرهای هیوسیامین، آتروپین نامیده میشود.
L-هیوسیامین شکل فعال و سمی مولکول است. از
آنجا که اغلب روشهای تجزیه در جداسازی
انانتیومرها توانایی چندانی ندارند، آتروپین بهعنوان
یک شاخص کلی L- (و D-) هیوسیامین در بیان مقدار سمیت گیاه در نظر گرفته میشود.
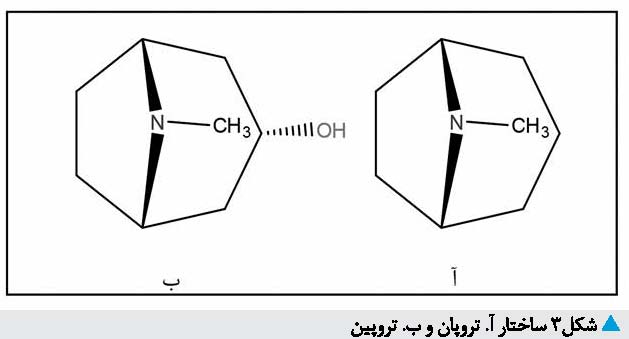
آلکالوییدهای تروپان از ساختار حلقهای آزابی سیکلو [3.2.1]اوکتان تشکیل شدهاند و طیف گستردهای
که از آنها در تیره
بادنجانیان شکل میگیرد،
در اثر واکنش با تروپین و انواع اسیدها به تولید استر میانجامد.

آنچه از سر، گذشت
آتروپا بلادونا5 (شابیزک)
گیاهی سمی از تیره بادنجانیان است. میوههای
گرد و آبدار آن، در آغاز سبزند و با گذشت زمان سیاه میشوند.
میوههای رسیده و برگهای سبز دارای بالاترین میزان سمهای آتروپین، هیوسیامین و اسکوپولامین
هستند. به علت شباهت میوه این گیاه با انواع توتها،
خطر مسمویت و حتی مرگ کودکان در اثر مصرف آن بسیار جدی است.
توهمزایی
از دیگر نشانههای شناخته شده مصرف
آتروپا بلادونا است تا جایی که در گذشته برای خوشگذرانیها در مراسم تشریفاتی مصرف میشد.
استفاده از نام آتروپا از آتروپوس6،
بزرگترین ایزدبانو در
میان الهههای سرنوشت که وظیفه
قطع ریسمان زندگی انسان را به عهده داشت، الهام گرفته شده است. واژه بلادونا نیز
ریشهای ایتالیایی به معنی
بانوی زیبا دارد. زنان اروپایی در قرن نوزدهم میلادی با بهکارگیری
عصاره میوه آتروپا بلادونا و درشت کردن مردمک چشمهایشان،
زیبایی خود را افزایش میدادند.
بهنظر میرسد به پیامدهای پرخطر این کار روی
بینایی اهمیت چندانی داده نمیشد.
نام آتروپا بلادونا را لینه7، گیاهشناس
سوئدی در سال 1753میلادی برگزید و در سال 1809 واکلین8 بهوجود آتروپین در آن پی برد. از این پس،
آتروپین بهطور ویژه، درکانون
توجه قرار گرفت، شیمیدانهای آلمانی اهمیت موضوع را بهخوبی درک کردند و پژوهشهای بسیاری در این زمینه انجام شد که
مهمترین آنها پژوهشهای
یک داروساز به نام مِین9 بود که در سال 1831 موفق به جداسازی بلورهای
خالص آتروپین شد.
آتروپین از نگاه
کارشناسی
عصبها
به کمک مواد شیمیایی که در فضای بین اعصاب پخش میشود
با یکدیگر ارتباط برقرار میکنند.
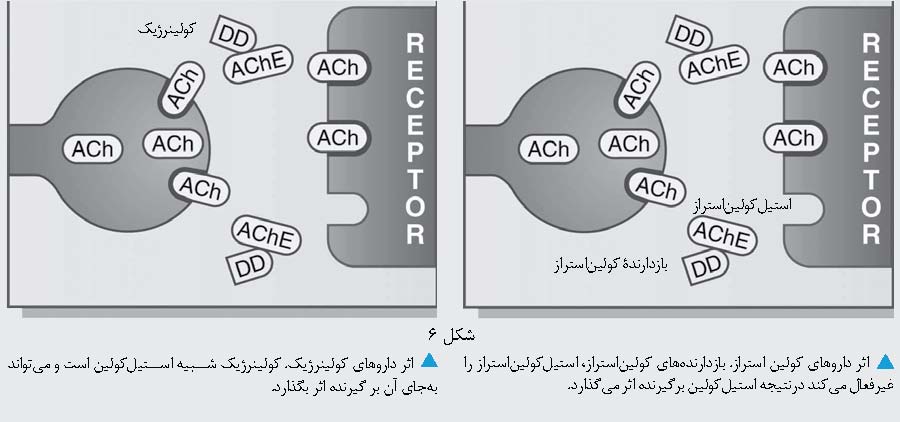
این مواد شیمیایی همان پیامرسانهای عصبی هستند که استیلکولین یکی از آنهاست.
مادهای که روی گیرندههای پیامرسان
عصبی استیلکولین اثر بازدارنده
دارد و از اثربخشی آن در سامانه عصبی مرکزی و محیطی جلوگیری میکند، آنتیکولینرژیک10
نامیده میشود. آتروپین و دی-
سیکلومین11 رایجترین
داروهای این طبقه هستند.
افزایش تعداد ضربان قلب به بیش از 100
ضربه در دقیقه، یکی از مهمترین
اثرهای شناختهشده آتروپین در سال
1867 بود. در پایان قرن نوزدهم ثابت شد که آتروپین مانع از عملکرد مادهای به نام موسکارین12 در
کاهش ضربان قلب میشود
و در سال 1921 میلادی لویی13 این نکته را دریافت که کاهش ضربان قلب،
ناشی از وجود ماده شیمیایی آزاد شده از عصب واگ است. چند سال بعد وی همراه ناوراتیل14
این ماده را استیلکولین
نامید. لویی خیلی زود به این واقعیت دستیافت
که آتروپین سدی محکم در برابر استیل کولین میسازد
و از فعالیت آن در بدن جلوگیری میکند.
حتی پیشتر در سال 1914،
پژوهشهای دانشمندی
بریتانیایی به نام دیل15 در عرصه پزشکی و داروسازی، اعتبار زیادی کسب
کرد. دیل به این نکته پی برد که استیلکولین
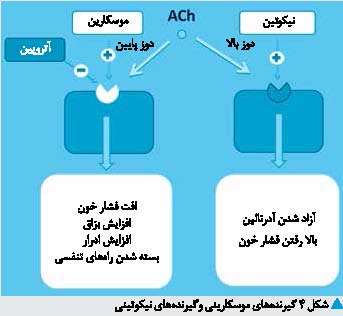
تزریقی، رفتاری دوگانه دارد. یک نوع این رفتار به وسیله موسکارین تقلید میشود و فعالیت آن در صورت حضور آتروپین،
پایان مییابد که وی آن را
موسکارینی نامید (گیرندههای
موسکارینی). نیکوتین، بهعنوان
یک جعلکننده دیگر هویت
استیلکولین، نسبت به
آتروپین غیرحساس بود که دیل، نام نیکوتینی را برای آن برگزید (گیرندههای نیکوتینی).
گفتنی است، موسکارین آلکالوییدی طبیعی
است که در بسیاری از قارچهای
خودرو یافت میشود و اگرچه هیچ
خاصیت درمانی ندارد، پیامدهای سمی آن چشمگیر است. چنانکه
اشاره شد، موسکارین همانند استیلکولین
در بدن رفتار میکند و آتروپین با تقلید
عمل استیلکولین و هر ماده
مشابه از جمله موسکارین، مانع از برقراری پیوند استیلکولین
با گیرندههایش میشود و خود در جایگاه گیرندههای آن مینشیند. این در حالی است که هیچگونه پاسخی از سلول مشاهده نمیشود. این روش، اساس کار آنتاگونیستهای رقابتی است. موسکارین بر گیرندههای نیکوتینی، بیاثر
و پایداری آن از استیلکولین
بیشتر است و بهراحتی در دستگاه
گوارش جذب میشود.
از آنجا که موسکارین، استر نیست، با
آنزیم کولیناستراز آبکافت نمیشود. بنابراین در صورت مسمومیت با آن
درمانهای پزشکی و مصرف
آتروپینسولفات مورد نیاز
است. در صورت عدم رسیدگی، مسمومیت با موسکارین میتواند
منجر به مرگ شود.
سنتز نهایی آتروپین از واکنش میان
تروپین با تروپیک اسید در حضور کلریدریک اسید و گرما به دست میآید. ریچارد ویلشتتر16 شیمیدان آلمانی برای نخستین بار این ماده را
در سال 1901 سنتز کرد. امروزه آتروپین دارویی رایج در نسخههای
پزشکی است که با هدفهای
درمانی مختلف تجویز میشود.
در مغز پزشکی
در میانه دهه 1800، استفاده از
آلکالوییدهای آتروپا بلادونا پیش از آنکه سازوکار آنها
درک شود و در حالی که هنوز ماهیت بیماری پارکینسون مشخص نبود، رواج داشت. آتروپین
و اسکوپولامین بهعنوان نخستین داروهای
مؤثر در درمان پارکینسون، باعث کاهش رعشه در این بیماری میشدند.
امروزه داروهای سنتزی مختلفی برای درمان پارکینسون در دسترس است که معروفترین آنها
با نام ال- دوپا 17در بازارهای تجاری دارو عرضه میشود.
آتروپین، گیرندههای
هیستامین (H2) را مسدود و از ترشح بیش از حد اسید معده
جلوگیری میکند و هنگام بیهوشی
در عملهای جراحی، با هدف به
حداقل رساندن ترشحات بزاق، که در تنفس بیمار اختلال ایجاد میکند،
کاربردی اساسی دارد. البته زمانی که داروی قویتری
مورد نیاز باشد، اسکوپولامین در اولویت قرار میگیرد.
کم شدن تعداد ضربان قلب به کمتر از 60 ضربه در دقیقه نیز از دیگر حالتهایی است که هنگام عملهای جراحی، شخص را با شرایط بحرانی روبهرو میکند.
در این هنگام، آتروپین به کمک بیمار میآید
و ضربان قلب را افزایش میدهد.
از ترکیب آتروپین با برخی از داروها،
پادزهری برای مسمومیتهای
ناشی از حشرهکشها و گازهای فلجکننده
اعصاب به دست میآید. در چنین شرایطی،
غلظت آتروپین بالا می رود و استیلکولین
را که عامل مسمومیت فرد است، متعادل و مسیر درمان را هموار میکند.
گزیدهای
از دیگر تجویزهای پزشکی آتروپین شامل درمانهای
زخم معده، انقباض و گرفتگی غیرارادی روده، بیماریهای
چشمی، اختلالهای دستگاه ادراری،
التهاب کیسه صفرا، سنگ کلیه، آسم، التهاب مفصل و سرماخوردگی است.
آتروپین، داروی نفوذی
این دارو با گذر از سد خونی- مغزی و
درگیر کردن دستگاه عصبی مرکزی، نقش خود را به نمایش میگذارد.
چگونگی برقراری پیوند دارو با پروتئینهای
موجود در پلاسما هنوز مشخص نیست. موضوع مهم دیگر این است که آتروپین در زمان
بارداری، به راحتی از جفت عبور میکند
و به جنین منتقل میشود.
در چنین شرایطی، نفوذ از سد خونی- مغزی محدودتر میشود.
پیامدهای ناخواسته
گاه آنچه از پاسخ یک دارو در بدن انتظار
میرود، واقع نمیشود و عوامل محیطی مانند دما، نور
خورشید و ارتفاع روی واکنش بدن اثر میگذارند.
در این میان، رژیم غذایی مهمترین
عاملی است که بهعنوان بخش جداییناپذیر زندگی انسان، جذب دارو در بدن را
با چالش روبهرو میکند. بنابراین زمانبندی وعدههای
غذایی و نوع غذا باید با دقت بیشتری در برنامه دارویی بیماران در نظرگرفته شود.
مصرف زیاد آتروپین، فرجامی تلخ به همراه
دارد تا آنجا که به مرگ فرد میانجامد.
گزارشهایی حاکی از مرگ افراد
در اثر مصرف قرصهای آتروپین و حتی
گیاهان دربردارنده این ماده، در سازمانهای
بهداشتی به ثبت رسیده است. از این رو، توصیه پزشکان در درمانهای
مبتنی بر آتروپین، مصرف مقدار کم دارو به ازای تعداد دفعات بیشتر است.
افزایش ضربان قلب، خشکی دهان و گلو،
یبوست، ناتوانی در دفع ادرار، اختلال در بلع، گشاد شدن مردمک چشم، برافروختگی
پوست، تهوع، سردرد، خشکی پوست، ورم شکم، کاهش یا افزایش فشار خون، ناتوانی جنسی،
کاهش تعریق که در پی آن، دمای بدن افزایش مییابد
که در محیطهای گرم تا 105 درجه
فارنهایت و بیشتر میرسد
و نورگریزی مهمترین اثرهای نامطلوب
این دارو در بدن هستند.
مسمومیت ناشی از آتروپین با استفاده از
داروی فیزوستیگمین18 برطرف میشود
که با تزریق آن بهصورت
داخل وریدی، به سرعت پیامدهای هذیانگویی
و بیهوشی آتروپین از میان میرود.
فیزوستیگمین یک داروی کولینرژیک است. ویژگی
برجسته این داروها، افزایش مقدار استیلکولین
در همسایگی گیرندههای
آن است. در نتیجه، مسدود شدن گیرندههای
موسکارینی با آتروپین، پایان مییابد.
زیست دگرگونی
آنتیکولینرژیکها به سرعت از خون خارج و در سراسر بدن
پخش میشوند. بهطور کلی با تزریق عضلانی، این داروها
سریعتر در بدن جذب میشوند. کبد مسئول تغییرات شیمیایی
داروهاست و کلیه، مسیر اصلی دفع آنها
بهشمار میرود. سوختوساز
آنتیکولینرژیکها به روشنی مشخص نشده است.
آتروپین از راه پوست، غشای مخاطی و دهان
به مصرف میرسد. در میان روشهای بیانشده،
تزریق داخل وریدی آتروپین در بدن زودتر عمل میکند.
شروع فعالیت این دارو به شکل قرص و از راه دهان، بین نیم تا یک ساعت است. این در
حالی است که این اثر با تزریق عضلانی بین 10 تا 30 دقیقه، و در تزریق داخل وریدی
آن بین 2 تا 4 دقیقه طول میکشد.
75 تا 95 درصد آتروپین جذبشده،
از راه ادرار دفع میشود.
بهطور تقریبی 13 تا 50
درصد از مقدار آتروپین یافت
شده در ادرار، بدون تغییر است. مقدار کمی از آن نیز در مدفوع خارج میشود و حتی مقدار کمتری در فرایند بازدم
هدر میرود. نیمهعمر کوتاه آتروپین به چهار ساعت میرسد.
داروهای مشابه
برخی از مهمترین
داروهای این دسته عبارتاند
از:
•
اسکوپولامین
اگرچه هیدروبرمیداسکوپولامین خواصی
مانند آتروپین از خود نشان میدهد،
تفاوتهایی هم با آن دارد.
ضربان قلب هنگام مصرف اسکوپولامین در مقایسه با آتروپین کمتر افزایش مییابد. این در حالی است که پیامد بزرگ
شدن مردمک در اثر اسکوپولامین شدیدتر
است. افزون بر این آتروپین، دستگاه عصبی مرکزی را تحریک میکند
و اسکوپولامین، درست در نقطه مقابل این رفتار، فعالیت قشر مغزی را کاهش میدهد.
اسکوپولامین آرامبخش
قویتری است از این رو،
بیشتر در دندانپزشکی استفاده میشود و کاربردیتر
از آتروپین است. هر چند خشک شدن دهان و گلو در نتیجه مصرف آن، بیشتر احساس میشود.
اثربخشی تزریق عضلانی اسکوپولامین پس از
10 تا 15 دقیقه آغاز میشود
و مدت زمان اثر آن 90 دقیقه طول میکشد.
از عارضههای احتمالی آن،
هیجان، بیحسی، عدم تمرکز و
هذیانگویی را میتوان برشمرد.
•
گلیکوپیرولات
این دارو در سال 1961 میلادی معرفی شد و
از بسیاری جنبهها با آتروپین و
اسکوپولامین، برابری و چه بسا بهتر هم عمل میکند.
هنگامی که به شکل تزریق عضلانی استفاده میشود،
عملکرد آن پس از 10 تا 15 دقیقه، درک و اوج اثربخشی در بازه زمانی 30 تا 45 دقیقه
نمایان میشود و اثر آن نزدیک
به 7 ساعت در بدن باقی میماند.
از آنجا که آمونیوم بخشی از
گلیکوپیرولات را تشکیل میدهد،
نمیتواند از غشاهای
چربی، مانند سد خونی- مغزی عبور کند، در حالی که آمینهای
نوع سوم همچون آتروپین و اسکوپولامین بهراحتی
از غشاهای چربی میگذرند
و خود را به دستگاه عصبی مرکزی میرسانند.
اگر به داروی گلیکوپیرولات بهعنوان
یک آرامبخش نگاه میکنید باید گفت، چنین اثری از خود نشان
نمیدهد. همچنین در بخش
پیامدهای ناشی از این دارو، هذیانگویی
ثبت نشده است.
در پی مصرف 2/0 میلیگرم گلیکوپیرولات، بیمار با خشک شدن
دهان روبهرو میشود، در حالی که این اثر با مصرف 4/0
میلیگرم از آتروپین رخ میدهد.
با وجود اینکه گلیکوپیرولات همانند
آتروپین و اسکوپولامین عامل افزایشدهنده
ضربان قلب است، این پیامد آن به شدت دیگر داروهای آنتیکولینرژیک
نیست و بیماران قلبی آن را با خیال آسودهتری
استفاده میکنند. همچنین در
دندانپزشکی هنگامی که
ضربان قلب باید به کندی افزایش یابد و خشک شدنهای
طولانیمدت دهان مورد نظر
است، گلیکوپیرولات جایگزینی مناسب برای آتروپین و اسکوپولامین است.
•
مپریدین
مپریدین نیز یکی دیگر از داروهای مشابه
آتروپین است که برای نخستین بار در دهه 1930 بهعنوان
یک داروی آنتیکولینرژیک شناخته شد.
2 تا 4 دقیقه پس از تزریق داخل وریدی آن، اثر درمانی دارو بروز میکند و مدت اثربخشی، 30 تا 45 دقیقه
ادامه مییابد. مپریدین ترشحات
بزاق را کاهش و ضربان قلب بیمار را افزایش میدهد.
این دارو پس از دریافت تأیید سازمان دارو و غذا، در سال 1942 در بازارهای جهانی
عرضه شد.
آتروپین و اسکوپولامین هم به ترتیب در
سالهای 1938 و 1939
میلادی بهطور رسمی از سوی
سازمان دارو و غذا تأیید شدند، اما خیلی پیشتر
از آن، کاربرد بالینی داشتند.
در بازار دارو
آتروپین، یکی از داروهای اصلی در فهرست
داروهای اساسی سازمان بهداشت جهانی، از داروهایی است که در مراقبتهای بهداشتی اولیه ضروری و مورد نیاز
است.
امروزه اگرچه میتوان
آلکالوییدهای تروپان بهویژه
آتروپین و اسکوپولامین را سنتز کرد، استخراج آنها
از گیاهان، به صرفهتر
است. گونههای شابیزک (آتروپا
بلادونا)، درخت چوبپنبهای استرالیا و بنگدانه
منابع اصلی مواد اولیه هستند و مهم است که
روشهایی اقتصادی و
کارآمد برای جداسازی این آلکالوییدها در نظر گرفته شوند.
با ورود تولیدکنندههای چین، هند و استرالیا به بازارهای
جهانی آلکالوییدهای تروپان خالص، تولیدکنندههای
آفریقایی باید تلاش بیشتری در پیش بگیرند تا بتوانند همچنان در این بازار حضور
داشته و پیروز این رقابت باشند.
پینوشتها
1.
tropane alkaloid 2.
erythroxylaceae 3. scopolamine
4.
L-hyoscyamine 5.Atropa belladonna 6. atropos
7. Linne
8.
Vacquelin 9. Mein 10.anticholinergic 11.dicyclomine
12.
muscarine 13. Loewi 14. Navratil 15. Dale
16. Willstätter, R. 17. l-dopa 18. physostigmine
منابع
1.
Dowd, F. J. et al. “Pharmacology and Therapeutics for Dentistry”, Elsevier -
Health Sciences Division, 2017.
2.
Kee, J. L. et al. “Pharmacology: A Patient-Centered Nursing Process Approach”,
Elsevier Health Sciences, 2015.
3.Adamse,
P. et al. “Tropane alkaloids in food: Poisoning incidents”, Quality Assurance
and Safety of Crops & Foods, 6, 15-24, 2014.
4.European
Food Safety Authority“Scientific Opinion on Tropane alkaloids in food and feed”
EFSA Journal, 11, 1-113, 2013.
5.
Berdai, A. et al. Pan African Medical Journal,2012, 11, 1.
6.
He, Y. et al. J. Sep. Sci., 2011,34, 806.
7.
Fidan, T. et al. Eurasian J Emerg
Med,2011, 10, 86.
8.
Malamed, S.F. “A CLINICAL Guide to Patient Management” Elsevier Health
Sciences,2010.
9.
Vardanyan, R. S. et al. “Synthesis of Essential Drugs” Elsevier, 2006.
10.
Webster R. “Neurotransmitters, Drugs and Brain Function” John Wiley & Sons,
2001.
11.
Florey, K. “Profiles of Drug Substances, Excipients and Related Methodology”
Academic Press, 1985.
12.
Simpson, L. L. “Neuropoisons; Their Pathophysiological Actions: Poisons of
animal origin” Plenum Press, 1974.
13.www.researchgate.net/publication/261477346-Datura_stramonium-
L, 2014.
14.
www.researchgate.net/ publication/ 254834358 _Tropane - alkaloids - in- food,
2010.