روش کار
ـ پیش از شروع کلاس، در یک ارلن 500
میلیلیتری، 100mL آب و یک قاشق چایخوری سدیم هیدروکسید یا پتاسیم
هیدروکسید بریزید.
ـ یک قاشق غذاخوری گلوکوز به این محلول
بیفزایید و آن را هم بزنید. توجه کنید که اگر از شکر استفاده شود، واکنش به خوبی
انجام نمیگیرد و تغییر رنگ مشخصی دیده
نمیشود.
ـ در پایان، دو یا سه قطره محلول متیلن
بلو به مخلوط درون ارلن بیفزایید و ارلن را با خود به کلاس ببرید.
ـ رنگ آبی تیره نظر دانشآموزان را جلب میکند و کنجکاوی آنها را برمیانگیزد.
ـ دهانه ارلن را ببندید و آن را روی میز
قرار دهید.
ـ پس از اعلام عنوان درس (گروههای عاملی در شیمی آلی)، توجه دانشآموزان را به رنگ ارلن جلب کنید که بیرنگ شده است.
ـ ارلن را تکان دهید. آبی تیره دوباره
ظاهر میشود.
ـ با رسم ساختار گلوکوز و شکل اکسایش
یافته آن، بدون توضیح در مورد جزئیات واکنش، گروههای عاملی را در آنها بررسی کنید.
ـ اجازه دهید دانشآموزان هم، رنگ آبی و بیرنگ شدن را در محلول ایجاد کنند.
این محلول را میتوانید برای چندین کلاس، حتی برای هفته
بعد استفاده کنید.

سازوکار واکنش
مقالههای زیادی تبدیل گلوکوز به شکل اسیدی
آن، گلوکونیک اسید را مورد بررسی قرار دادهاند.
بنا به دادهها، واکنش نسبت به اکسیژن،
از مرتبه صفر برخوردار است . ورینن1 توانست کاهش گلوکوز را
با توجه به شکلهای انولی در محیط بازی
توجیه کند:
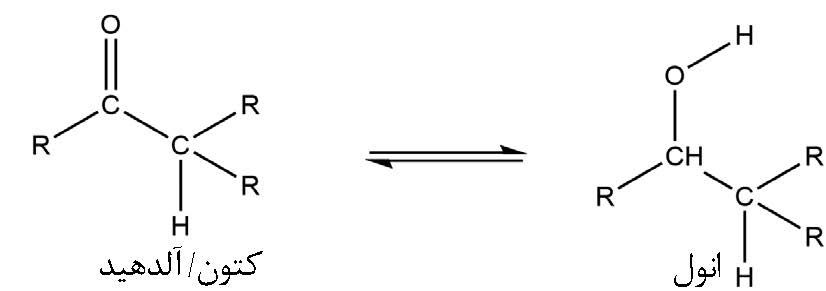
بنا به این نظریه ـ که با بررسیهای لارن2 نیز تأیید میشود ـ واکنش با انولدار شدن گلوکوز و تبدیل شدن به یون آغاز
میشود:
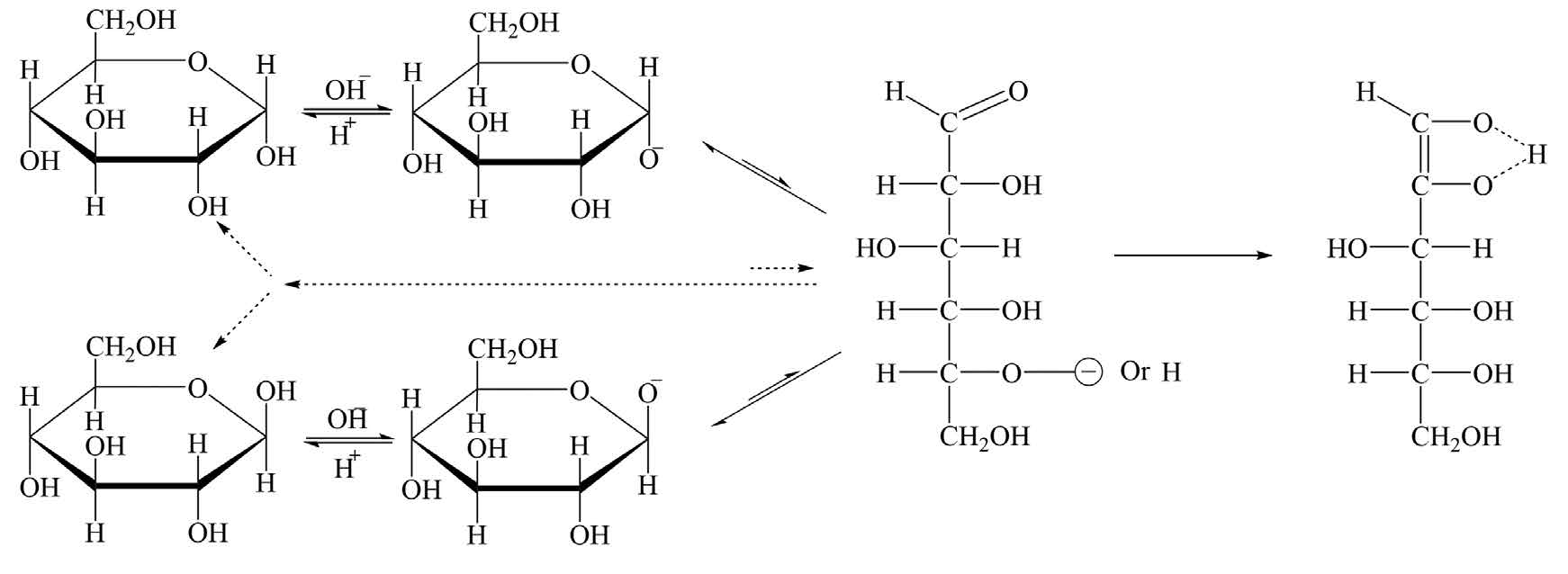
سپس متیلن بهعنوان مادهای کاهنده در محیط این واکنش، با گرفتن
الکترون به متیلن سفید یا بیرنگ تبدیل میشود:
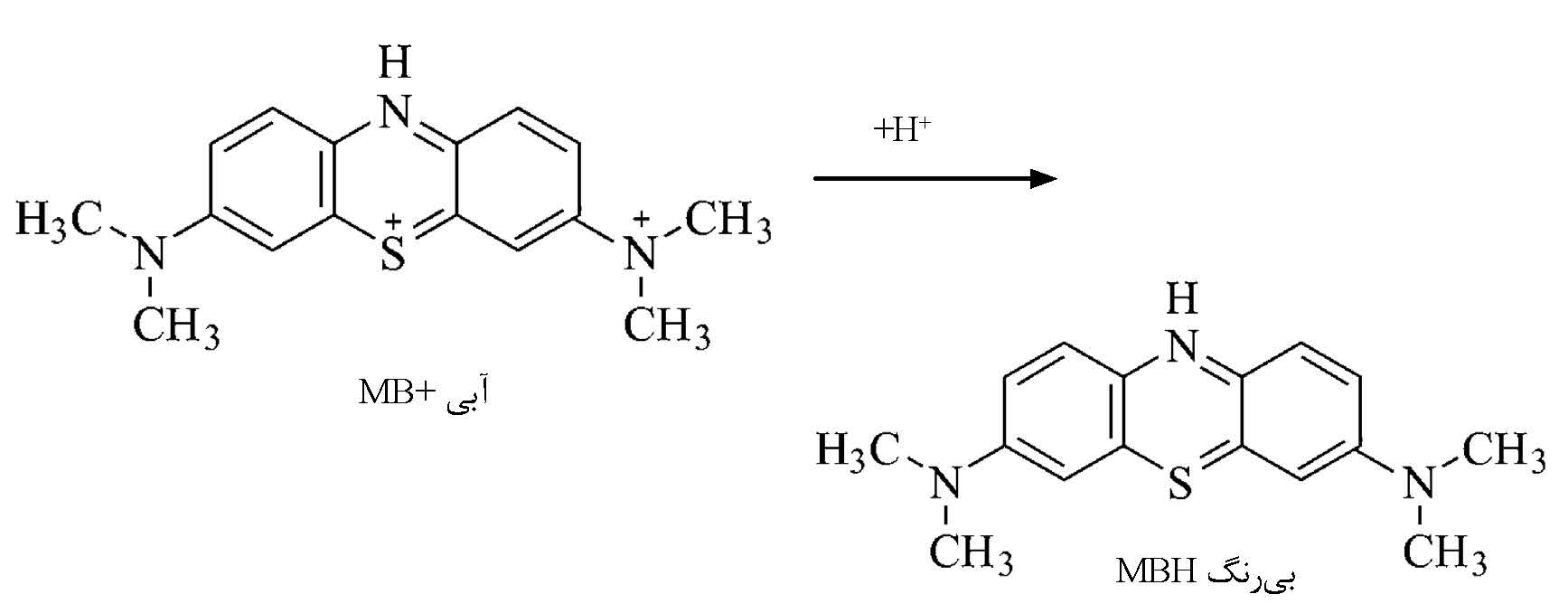
بیدرنگ مرحله دوم واکنش آغاز میشود و اکسیژن محلول در آب، متیلن سفید
را دوباره اکسید، و به شکل آبیرنگ آن تبدیل میکند. اگر اکسیژن محلول تمام شود، رنگ
محیط واکنش سفید (بیرنگ) باقی میماند مگر اینکه ظرف واکنش را هم بزنیم
تا باز هم اکسیژن محلول تولید شود.

کمبل3 استفاده از آزمایش
بطری آبی را برای تدریس مبحث سینتیک پیشنهاد کرد. لارن و همکارانش نیز مرحله تعیینکننده در سرعت واکنش را بررسی کردند.
علاقهمندان برای بررسی ارتباط بیشتر این
آزمایش با مبحث سنتیک، میتوانند منبع 2 را مطالعه
کنند. هدف از آوردن این آزمایش در کتاب درسی، فقط جلب توجه دانشآموزان و ایجاد انگیزه است و نیازی به
مطرح کردن جزئیات نیست.
پینوشتها
1.Vourinen,T.
2.Laurens,A.
3.Campbell,J.
منابع
1. زهرا ارزانی، آزمایش بطری آبی، مجله رشد
آموزش شیمی، 1378، شماره 56.
2. Laurens, A.
et al. J. Chem. Educ., 2012, 89 (11), 1425.
3. Campbell, J.
A. J. Chem. Educ. 1963, 40, 578.
4.
Adamčíková, L.; Pavlíková, K.; Ševčík, P. Int. J. Chem. Kinet. 1999, 31,
463.
5. Vuorinen, T.
Carbohydr. Res. 1983, 116, 61.
6.
www.rsc.org/learn-chemistry/resource/res00000729/the-blue-bottle-experiment?cmpid=CMP00005928
7.eic.rsc.org/exhibition-chemistry/the-blue-bottle-reaction/2020070.article
8.
/faculty.mansfield.edu/bganong/biochemistry/bluebott.htm
9.www.csun.edu/scied/2-chem/redox_methylene_blue/index.htm