مقدمه
به کمک مدل کوانتومی اتم میتوانیم چگونگی آرایش الکترونها در اتم را تعیین کنیم. الکترونها همواره تمایل دارند تا در پایینترین تراز انرژی قرار گیرند یا اوربیتالی را زودتر پر کنند که سطح انرژی آن پایینتر است (طرح آفبا). از آنجا که یادگیری و حفظ ترتیب پر شدن زیرلایهها برای دانشآموزان چالش بزرگی است در این مقاله، یادگیری ترتیب پر شدن زیرلایهها به روشی بسیار ساده، جذاب، کاربردی و در مدتزمان کوتاه و همچنین رسم آرایش الکترونی اتمهایی با عدد اتمی کوچک و بزرگ مورد بررسی قرار میگیرد.
روش اجرا
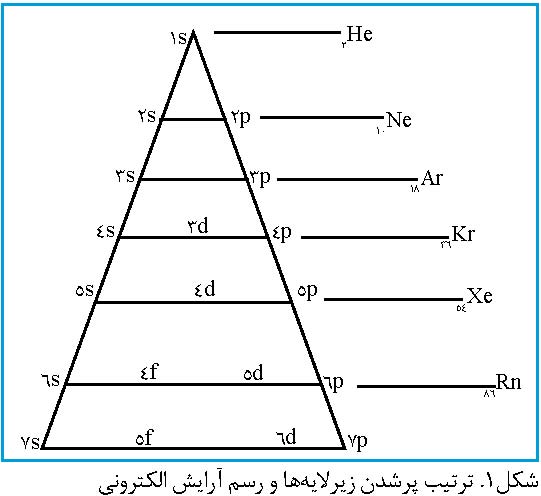
پس از اینکه دانشآموزان با مفاهیم عددهای کوانتومی و توزیع الکترونها در لایهها و زیرلایهها آشنا شدند، این روش اجرا میشود. نخست مانند آنچه در شکل۱ دیده میشود مثلثی شامل خطوط افقی برای نمایش 7....1،2=n رسم میکنیم. عددهای ۱ تا ۷ را از رأس مثلث در دو سمت چپ و راست قرار میدهیم. میبینید که با گذاشتن s، در کنار عددهای سمت چپ، کار با نخستین عدد کوانتومی روی شکل تمام شده است. اکنون در کنار عددهای سمت راست مثلث، حرف p را به عنوان دومین عدد کوانتومی فرعی قرار میدهیم. برای عدد کوانتومی بعدی یعنی d و اوربیتال f، از داخل مثلث استفاده میکنیم. با توجه به جدول تناوبی، اوربیتال 3d در عنصرهای تناوب چهارم در حال پرشدن است. پس روی خط مربوط به تناوب چهارم تا هفتم، اوربیتالهای d را قرار میدهیم و آنها را به ترتیب، با شماره 3 تا 6 مشخص میکنیم. حالا نوبت به اوربیتال 4f میرسد. با توجه به جدول در تناوب ششم، اوربیتال 4f شروع به پرشدن میکند. پس روی دو خط مربوط به تناوب شش و هفت، این اوربیتال را مشخص میکنیم و به ترتیب، شمارههای ۴ و ۵ را در کنار آنها میگذاریم. اگر این مثلث را در ذهن داشته باشیم به راحتی میتوانیم آرایش الکترونی اتمهای مختلف را با شروع از رأس مثلث و به ترتیب، پر کردن زیرلایهها از خطی به خط دیگر، در کوتاهترین زمان رسم کنیم.
آرایش الکترونی اتمها را به شیوه دیگری نیز میتوان نوشت که آرایش الکترونی فشرده نام دارد. در این آرایش الکترونی نماد شیمیایی گاز نجیب پیش از اتم مورد نظر را داخل کروشه قرار میدهیم، سپس با استفاده از شکل ۱، شروع به پر کردن زیرلایهها میکنیم.
16S :[Ne] 3s3 2p4
35Br :[Ar] 3d4 10s4 2p5
72Hf :[Xe] 4f5 14d6 2s2
توجه
در این روش برای رسم آرایش الکترونی هافنیم با توجه به شکل مثلث، پس از نوشتن گاز نجیب زنون ـ که در دوره پنجم قرار دارد ـ عدد زیرلایهها را از کوچک به بزرگ مینویسیم (۴ و ۵ و ۶) اما برای پر کردن الکترون در زیرلایهها با توجه به شکل مثلث، ترتیب قرار گرفتن زیرلایهها را رعایت میکنیم. یعنی در آغاز ۲ الکترون در 6s، سپس ۱۴ الکترون در 4f، و در انتها ۲ الکترون در 5d قرار میدهیم.
آرایش الکترونی شرایط خاص
قاعده آفبا، آرایش الکترونی اغلب عنصرها را به خوبی پیشبینی میکند ولی برای برخی عنصرهای جدول، نارسایی دارد. روشهای پیچیده طیفسنجی که آرایش الکترونی اتمها را با دقت تعیین میکند، نشان میدهد که اتمهای کروم و مس هریک در بیرونیترین زیرلایه خود فقط یک الکترون دارند.
24Cr :[Ar] 3d4 5s1
24Cr :[Ar] 3d4 4s2
29Cu :[Ar] 3d4 10s1
29Cu :[Ar] 3d4 9s2
بررسیهای دقیق طیفسنجی نشان میدهد که دو عنصر نقره و مولیبدن هم هر یک در بیرونیترین زیرلایه خود فقط یک الکترون دارند.
42Mo :[Kr] 4d5 5s1
42Mo :[Kr] 4d5 4s2
47Ag :[kr] 4d5 10s1
47Ag :[kr] 4d5 9s2
نتیجهگیری
در این تجربه آموزشی با استفاده از یک شکل بسیار ساده:
ـ یادگیری ترتیب پرشدن زیرلایهها به روش بسیار ساده و نوین آموزش داده شد.
ـ رسم آرایش الکترونی اتمها، بهویژه اتمهایی که دارای عدد اتمی بزرگ هستند و حفظ ترتیب پرشدن آنها که چالشی و طاقتفرسا بود، به صورت آسان و کاربردی بیان شد.
ـ رسم آرایش الکترونی اتمها بهصورت فشرده توضیح داده شد.
ـ آرایش الکترونی اتمها در شرایط خاص بیان شد.
ـ دانشآموزان در کمترین زمان ممکن توانستند آرایش الکترونی اتمها را رسم کنند.
ـ این روش نه تنها برای دانشآموزان پایه دهم، بلکه برای دانشآموزان کنکوری سودمند و کاربردی است.
این نتایج با توجه به پاسخ درست دانشآموزان به پرسشهای مفهومی و متنوع هنگام تدریس، پرسش آزمونهای پایانی و کنکور بهدست آمد و نشان داد که دانشآموزان به درک بهتری از مفاهیم مربوط به رسم آرایش الکترونی در مدت زمان کوتاه دستیافتهاند.